Step 4 of 6
Doppler couleur
Zone d’accélération concentrique (PISA)
Lorsqu’elles doivent passer d’une large cavité à une zone étroite, les molécules de fluide accélèrent en une zone concentrique en amont du rétrécissement, puisque les fluides sont incompressibles. Cette zone de convergence hémisphérique est d’autant plus grande que l’accélération est élevée, donc que la quantité de liquide qui doit transiter par l’orifice est importante. Cette zone est appelée proximal isovelocity surface area, ou PISA, parce que la vitesse du fluide est la même sur la toute la surface de chaque hémisphère concentrique successif [4,7,8,9]. Selon l’équation de continuité, le produit de la vélocité à la surface d’un hémisphère et de la surface de cet hémisphère est égal au produit de la vélocité maximale à travers l’orifice et de la surface de ce dernier :
(S • V)Hémisphère = (S • V)Orifice
La surface d’un hémisphère est la moitié de celle d’une sphère : S = (4 π • r2) / 2, soit : 2 π • r2. En accélérant en zones concentriques, le flux visible au Doppler couleur franchit la limite de Nyquist (recouvrement spectral ou aliasing) et change de couleur : il passe d’une extrémité à l’autre de l’échelle de couleur. Dans le cas d’une insuffisance mitrale, par exemple, le flux passe du rouge au jaune en accélérant en direction du capteur, puis saute au bleu (Vidéo et Figure 25.164). Ce passage d’une extrémité à l’autre de l’échelle de couleur permet de connaître la vélocité qui règne à la surface de cet hémisphère : c’est la vélocité d’aliasing, indiquée au sommet de l’échelle de couleur (40-50 cm/s). Le produit de cette vélocité et de la surface de cet hémisphère peut être utilisé dans l’équation de continuité pour calculer l’orifice de régurgitation (OR), puisque tout le sang qui passe par le PISA traverse l'orifice de régurgitation : SHémisph • VAliasing = SOrifice • VmaxRégurg. D’où :
S orifice de régurgitation = (SHémisph • VAliasing) / VmaxRégurg
= (6.28 r2 • VAliasing) / VmaxRégurg

Figure 25.164 : Zone d’accélération concentrique proximale (PISA) illustrée dans une insuffisance mitrale en vue mi-oesophagienne rétrocardiaque. A : représentation schématique ; le PISA est un hémisphère concentrique centré sur l’orifice et situé dans la chambre d’amont du flux ; la vena contracta est la zone la plus étroite du flux laminaire qui sort du rétrécissement. B : en accélérant progressivement en direction de l’orifice, le flux Doppler franchit la limite de Nyquist (aliasing) et change de couleur ; il passe de l’extrémité jaune de l’échelle de couleur à l’extrémité bleue. Plus la Vmax est haute et plus le volume de sang à faire passer par l’orifice est élevé, plus la dimension du PISA est grande. C : image d’une insuffisance mitrale sévère ; lorsque l’échelle de couleur est réglée à 35-50 cm/s (ici 41 cm/s), un rayon de 1er aliasing (flèche blanche) de 1 cm correspond à une surface de l’orifice de régurgitation de 0.5 cm2 (IM sévère).
Vidéo: zone d'accélération concentrique (PISA) côté ventriculaire d'une insuffisance mitrale centrale; en accélérant, le flux passe du rouge au jaune puis au bleu.
Sur l’image gelée à l’écran, on peut supprimer la couleur pour ne faire apparaître que les structures bidimensionnelles afin de mieux localiser le centre de l’orifice de régurgitation. La mesure du rayon de l’hémisphère de 1er aliasing se fait entre ce point et celui où la couleur saute d’une extrémité à l’autre de l’échelle ; on choisit un rayon qui est dans l’axe du faisceau Doppler.
Dans l’insuffisance mitrale, on peut simplifier le calcul en clinique : si l’échelle de couleur est réglée sur une vélocité d’aliasing de 50 cm/s, un rayon de 1 cm pour l’hémisphère de 1er aliasing équivaut à un orifice de régurgitation ≥ 0.5 cm2, ce qui correspond à une IM sévère [5,12]. En effet :
S orifice de régurgitation = (6.28 • 1 cm2 • 50 cm/s) / 500 cm/s
S orifice de régurgitation (SOR) = 0.628 cm2
Une échelle de vélocité plus élevée donne un PISA plus petit et sous-estime l’importance de l’IM. Pour obtenir une vélocité d’aliasing de 40-50 cm/s dans le sens du flux, on peut également déplacer la ligne de base de l’échelle couleur dans la direction du jet [3]. La surface de l'orifice de régurgitation (SOR) est la quantification fondamentale de l'insuffisance valvulaire, alors que le volume de régurgitation est la meilleure mesure de la surcharge pour le ventricule [12].
Deux autres mesures sont faciles à déduire des calculs précédents. En multipliant la SOR par l’ITV de l’IM, on obtient le volume régurgité (VR). En rapportant le VR au volume systolique, on obtient la fraction de régurgitation (FR).
Vrég = SOR • ITVrégurg
FR = (Vrég / VS) • 100
Le calcul du PISA repose sur un certain nombre d’approximations qui peuvent ne pas être justes dans beaucoup de cas [9,12].
Lorsqu’elles doivent passer d’une large cavité à une zone étroite, les molécules de fluide accélèrent en une zone concentrique en amont du rétrécissement, puisque les fluides sont incompressibles. Cette zone de convergence hémisphérique est d’autant plus grande que l’accélération est élevée, donc que la quantité de liquide qui doit transiter par l’orifice est importante. Cette zone est appelée proximal isovelocity surface area, ou PISA, parce que la vitesse du fluide est la même sur la toute la surface de chaque hémisphère concentrique successif [4,7,8,9]. Selon l’équation de continuité, le produit de la vélocité à la surface d’un hémisphère et de la surface de cet hémisphère est égal au produit de la vélocité maximale à travers l’orifice et de la surface de ce dernier :
(S • V)Hémisphère = (S • V)Orifice
La surface d’un hémisphère est la moitié de celle d’une sphère : S = (4 π • r2) / 2, soit : 2 π • r2. En accélérant en zones concentriques, le flux visible au Doppler couleur franchit la limite de Nyquist (recouvrement spectral ou aliasing) et change de couleur : il passe d’une extrémité à l’autre de l’échelle de couleur. Dans le cas d’une insuffisance mitrale, par exemple, le flux passe du rouge au jaune en accélérant en direction du capteur, puis saute au bleu (Vidéo et Figure 25.164). Ce passage d’une extrémité à l’autre de l’échelle de couleur permet de connaître la vélocité qui règne à la surface de cet hémisphère : c’est la vélocité d’aliasing, indiquée au sommet de l’échelle de couleur (40-50 cm/s). Le produit de cette vélocité et de la surface de cet hémisphère peut être utilisé dans l’équation de continuité pour calculer l’orifice de régurgitation (OR), puisque tout le sang qui passe par le PISA traverse l'orifice de régurgitation : SHémisph • VAliasing = SOrifice • VmaxRégurg. D’où :
S orifice de régurgitation = (SHémisph • VAliasing) / VmaxRégurg
= (6.28 r2 • VAliasing) / VmaxRégurg
Figure 25.164 : Zone d’accélération concentrique proximale (PISA) illustrée dans une insuffisance mitrale en vue mi-oesophagienne rétrocardiaque. A : représentation schématique ; le PISA est un hémisphère concentrique centré sur l’orifice et situé dans la chambre d’amont du flux ; la vena contracta est la zone la plus étroite du flux laminaire qui sort du rétrécissement. B : en accélérant progressivement en direction de l’orifice, le flux Doppler franchit la limite de Nyquist (aliasing) et change de couleur ; il passe de l’extrémité jaune de l’échelle de couleur à l’extrémité bleue. Plus la Vmax est haute et plus le volume de sang à faire passer par l’orifice est élevé, plus la dimension du PISA est grande. C : image d’une insuffisance mitrale sévère ; lorsque l’échelle de couleur est réglée à 35-50 cm/s (ici 41 cm/s), un rayon de 1er aliasing (flèche blanche) de 1 cm correspond à une surface de l’orifice de régurgitation de 0.5 cm2 (IM sévère).
Vidéo: zone d'accélération concentrique (PISA) côté ventriculaire d'une insuffisance mitrale centrale; en accélérant, le flux passe du rouge au jaune puis au bleu.
Sur l’image gelée à l’écran, on peut supprimer la couleur pour ne faire apparaître que les structures bidimensionnelles afin de mieux localiser le centre de l’orifice de régurgitation. La mesure du rayon de l’hémisphère de 1er aliasing se fait entre ce point et celui où la couleur saute d’une extrémité à l’autre de l’échelle ; on choisit un rayon qui est dans l’axe du faisceau Doppler.
Dans l’insuffisance mitrale, on peut simplifier le calcul en clinique : si l’échelle de couleur est réglée sur une vélocité d’aliasing de 50 cm/s, un rayon de 1 cm pour l’hémisphère de 1er aliasing équivaut à un orifice de régurgitation ≥ 0.5 cm2, ce qui correspond à une IM sévère [5,12]. En effet :
S orifice de régurgitation = (6.28 • 1 cm2 • 50 cm/s) / 500 cm/s
S orifice de régurgitation (SOR) = 0.628 cm2
Une échelle de vélocité plus élevée donne un PISA plus petit et sous-estime l’importance de l’IM. Pour obtenir une vélocité d’aliasing de 40-50 cm/s dans le sens du flux, on peut également déplacer la ligne de base de l’échelle couleur dans la direction du jet [3]. La surface de l'orifice de régurgitation (SOR) est la quantification fondamentale de l'insuffisance valvulaire, alors que le volume de régurgitation est la meilleure mesure de la surcharge pour le ventricule [12].
Deux autres mesures sont faciles à déduire des calculs précédents. En multipliant la SOR par l’ITV de l’IM, on obtient le volume régurgité (VR). En rapportant le VR au volume systolique, on obtient la fraction de régurgitation (FR).
Vrég = SOR • ITVrégurg
FR = (Vrég / VS) • 100
Le calcul du PISA repose sur un certain nombre d’approximations qui peuvent ne pas être justes dans beaucoup de cas [9,12].
- L’orifice de régurgitation a une certaine dimension et n'est pas infiniment petit comme le suppose la formule mathématique. De ce fait, les hémisphères tendent à s’aplatir dans le voisinage immédiat de l’orifice. Le calcul n’est valide que si le rayon de l’hémisphère est au moins le double de celui de l’orifice. La forme du PISA n’est hémisphérique que lorsque le rayon est compris entre 10 et 15 mm.
- L’orifice de régurgitation est rarement circulaire; or un orifice ovale ou irrégulier entraîne une déformation elliptique des hémisphères. L'analyse tridimensionnelle du PISA donne une valeur de SOR environ 20% plus élevée que la mesure bidimensionnelle [11]. Dans l'IM fonctionnelle, l'orifice présente une forme en fente; l'imagerie 3D corrige la sous-estimation de l'orifice de régurgitation par l'analyse 2D, même si celle-ci comprend la mesure dans 2 plans orthgogonaux [1].
- La méthode du PISA ne permet pas de calculer la surface d’orifices multiples.
- La mesure du rayon de l’hémisphère d’aliasing doit se faire dans l’axe du faisceau Doppler ; ceci est facile dans une IM centrale, mais devient douteux dans une IM excentrique.
- La mesure du rayon du PISA et celle de la Vmax de l'insuffisance doivent avoir lieu au même moment de la phase de régurgitation, car une insuffisance évolue au cours de la systole (IM) ou de la diastole (IA); elle se renforce en télésystole dans les IM organiques (prolapsus), mais diminue en mésosystole dans les IM fonctionnelles [2].
- Comme le calcul du PISA fournit le flux instantané maximal, la valeur obtenue pour la surface de l’orifice de régurgitation est sa valeur maximale, qui peut être légèrement supérieure à celle obtenue par d’autres méthodes.
- L’insuffisance mitrale peut ne pas être pansystolique, comme c'est le cas dans celle liée à l'obstruction dynamique de la CCVG qui débute en mésosystole seulement. Le volume régurgité est donc plus faible pour la même image couleur télésystolique.
Dans la sténose mitrale, la valve a en général une forme de cône, et les hémisphères du PISA qui se forment du côté auriculaire en diastole ne sont plus complets ; il faut alors corriger la formule en la multipliant par l'angle (α) de ce cône dans le plan de coupe: (6.28 r2 • Valiasing / Vmax IM) • α / 180 (Figure 25.165) [6]. La même correction doit être apportée à une IM si les feuillets forment un angle entre eux en systole.
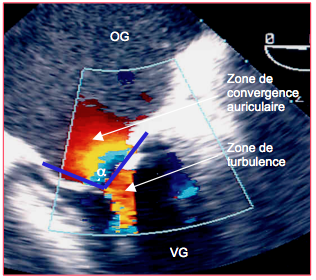
Figure 25.165 : Flux Doppler couleur dans une sténose mitrale. On voit une zone d’accélération concentrique diastolique sur le versant auriculaire de la valve (PISA) et un flux tourbillonnaire entre les feuillets. Le cône formé par les feuillets fusionnés est défini par son angle α qui doit être pris en compte dans le calcul de la surface d'ouverture de la sténose.
La surface d'ouverture de la sténose mitrale (SM) se calcule comme précédemment en divisant le produit de la surface et de la vélocité d'aliasing par la vélocité maximale du flux diastolique à travers la sténose:
S = (6.28 • r2 • VAliasing) / VmaxSM
Vena contracta
Dans un rétrécissement, le flux tend à couler dans la partie centrale car les zones externes sont freinées par le frottement contre les parois. Le flux est laminaire et le reste à sa sortie ; il ne devient turbulent qu'à quelque distance. Son plus petit diamètre n’est pas dans l’orifice lui-même, mais juste après, à un endroit appelé en hydrodynamique vena contracta (Figure 25.166) [10,12]. Ce phénomène survient avec tous les liquides passant à travers un orifice rétréci. La distance entre l'orifice et la zone la plus étroite du jet (distance 1-2 dans la figure) varie avec la vitesse du liquide, avec sa densité, avec la taille de l'orifice et avec la nature de la cavité de réception. Pour le sang à travers une sténose ou une insuffisance valvulaire, elle est de quelques millimètres. Comme le flux sanguin y est encore laminaire, la dimension de cette zone reproduit fidèlement la forme du flux dans la sténose, mais sa surface de section est légèrement plus petite que celle de l'orifice anatomique (GOA, geometrical orifice area). La mesure du diamètre de la vena contracta est une excellente technique pour évaluer la dimension de l’orifice effectif d'une sténose ou d'une régurgitation valvulaire (EOA, effective orifice area), car elle est indépendante de la vitesse du flux et de la pression motrice. De ce fait, elle garde sa valeur dans les insuffisances aiguës, où l’absence de dilatation de la cavité d’aval conduit à une rapide égalisation des pressions et où la dysfonction ventriculaire diminue la vélocité du jet, donc sa surface apparente. La dimension de la vena contracta est mieux corrélée à l'impact hémodynamique et au pronostic que la surface anatomique de l'orifice. L'insuffisance est sévère lorsque le diamètre de la vena contracta est > 0.7 cm dans le cas d’une IM ou d'une IT, et > 0.6 cm dans le cas d'une IA [12]. Toutefois, l'insuffisance mitrale est de nature dynamique, et son importance varie au cours de la systole; la taille de la vena contracta augmente en télésystole dans les insuffisances organiques (prolapsus), mais diminue en mésosystole dans les insuffisances fonctionnelles [2]. D'autre part, l'orifice de régurgitation mitrale se présente le plus souvent comme une fente plus ou moins elliptique et non comme un cercle. Alors que l'imagerie bidimensionnelle base tous ses calculs sur une surface circulaire, l'échocardiographie tridimensionnelle permet de reconstituer la forme réelle du jet d'IM et de mesurer la surface en coupe de la vena contracta. Cette mesure est la méthode la plus fiable de quantifier une insuffisance valvulaire [12].

Figure 25.166 : Vena contracta (VC) illustrée dans une insuffisance mitrale en vue mi-oesophagienne rétrocardiaque. A : La section de la vena contracta (1) est un peu plus petite que celle de l'orifice anatomique (2). B: Insuffisance mitrale mineure-à-modérée: La vena contracta et la zone d'accélération concentrique (PISA) sont étroites. C: en imagerie tri-dimensionnelle, le Doppler couleur permet d'évaluer le jet d'IM dans l'espace et de mesurer sa surface dans une coupe perpendiculaire à sa direction; dans le cas présent, la surface n'est pas circulaire mais elliptique.
© CHASSOT PG, BETTEX D. Avril 2019; dernière mise à jour, Mars 2020
Références
Figure 25.165 : Flux Doppler couleur dans une sténose mitrale. On voit une zone d’accélération concentrique diastolique sur le versant auriculaire de la valve (PISA) et un flux tourbillonnaire entre les feuillets. Le cône formé par les feuillets fusionnés est défini par son angle α qui doit être pris en compte dans le calcul de la surface d'ouverture de la sténose.
La surface d'ouverture de la sténose mitrale (SM) se calcule comme précédemment en divisant le produit de la surface et de la vélocité d'aliasing par la vélocité maximale du flux diastolique à travers la sténose:
S = (6.28 • r2 • VAliasing) / VmaxSM
| Zone d’accélération concentrique (PISA) |
| La dimension du PISA est proportionnelle à la quantité de sang qui traverse l’orifice (insuffisance, shunt) Surface de l’orifice = (6.28 r2 • VAliasing) / VmaxFlux où V et r sont la vélocité et le rayon du 1er aliasing (limite de Nyquist : 40-50 cm/s) Pour l’IM, un rayon de 1er aliasing > 1 cm signe un orifice de régurgitation > 0.5 cm2 (IM sévère) |
Vena contracta
Dans un rétrécissement, le flux tend à couler dans la partie centrale car les zones externes sont freinées par le frottement contre les parois. Le flux est laminaire et le reste à sa sortie ; il ne devient turbulent qu'à quelque distance. Son plus petit diamètre n’est pas dans l’orifice lui-même, mais juste après, à un endroit appelé en hydrodynamique vena contracta (Figure 25.166) [10,12]. Ce phénomène survient avec tous les liquides passant à travers un orifice rétréci. La distance entre l'orifice et la zone la plus étroite du jet (distance 1-2 dans la figure) varie avec la vitesse du liquide, avec sa densité, avec la taille de l'orifice et avec la nature de la cavité de réception. Pour le sang à travers une sténose ou une insuffisance valvulaire, elle est de quelques millimètres. Comme le flux sanguin y est encore laminaire, la dimension de cette zone reproduit fidèlement la forme du flux dans la sténose, mais sa surface de section est légèrement plus petite que celle de l'orifice anatomique (GOA, geometrical orifice area). La mesure du diamètre de la vena contracta est une excellente technique pour évaluer la dimension de l’orifice effectif d'une sténose ou d'une régurgitation valvulaire (EOA, effective orifice area), car elle est indépendante de la vitesse du flux et de la pression motrice. De ce fait, elle garde sa valeur dans les insuffisances aiguës, où l’absence de dilatation de la cavité d’aval conduit à une rapide égalisation des pressions et où la dysfonction ventriculaire diminue la vélocité du jet, donc sa surface apparente. La dimension de la vena contracta est mieux corrélée à l'impact hémodynamique et au pronostic que la surface anatomique de l'orifice. L'insuffisance est sévère lorsque le diamètre de la vena contracta est > 0.7 cm dans le cas d’une IM ou d'une IT, et > 0.6 cm dans le cas d'une IA [12]. Toutefois, l'insuffisance mitrale est de nature dynamique, et son importance varie au cours de la systole; la taille de la vena contracta augmente en télésystole dans les insuffisances organiques (prolapsus), mais diminue en mésosystole dans les insuffisances fonctionnelles [2]. D'autre part, l'orifice de régurgitation mitrale se présente le plus souvent comme une fente plus ou moins elliptique et non comme un cercle. Alors que l'imagerie bidimensionnelle base tous ses calculs sur une surface circulaire, l'échocardiographie tridimensionnelle permet de reconstituer la forme réelle du jet d'IM et de mesurer la surface en coupe de la vena contracta. Cette mesure est la méthode la plus fiable de quantifier une insuffisance valvulaire [12].
Figure 25.166 : Vena contracta (VC) illustrée dans une insuffisance mitrale en vue mi-oesophagienne rétrocardiaque. A : La section de la vena contracta (1) est un peu plus petite que celle de l'orifice anatomique (2). B: Insuffisance mitrale mineure-à-modérée: La vena contracta et la zone d'accélération concentrique (PISA) sont étroites. C: en imagerie tri-dimensionnelle, le Doppler couleur permet d'évaluer le jet d'IM dans l'espace et de mesurer sa surface dans une coupe perpendiculaire à sa direction; dans le cas présent, la surface n'est pas circulaire mais elliptique.
| Vena contracta |
| Zone de flux laminaire à vélocité maximale située immédiatement en aval de l’orifice (sténose, insuffisance, shunt) et en reproduisant la surface. Ses dimensions sont proportionnelles à celles de l’orifice de passage. Sa surface de section mesurée en reconstruction 3D est le moyen le plus fiable de quantifier une insuffisance valvulaire |
© CHASSOT PG, BETTEX D. Avril 2019; dernière mise à jour, Mars 2020
Références
- ASHIKHMINA E, SHOOK D, COBEY F, et al. Three-dimensional versus two-dimensional echocardiographic assessment of functional mitral regurgitation proximal isovelocity surface area. Anesth Analg 2015; 120:534-42
- COBEY FC, ASHIHKMINA E, EDRICH T, et al. The mechanism of mitral regurgitation influences the temporal dynamics of the vena contracta area as measured with color flow Doppler. Anesth Analg 2016; 122:321-9
- LAMBERT AS. Proximal isovelocity surface area should be routinely measured in evaluating mitral regurgitation: A core review. Anesth Analg 2007; 105:940-3
- LANCELLOTTI P, TRIBOUILLOY C, HAGENDORFF A, et al. Recommendations for the echocardiographic assessment of native valvular regurugitation: an executive summary from the EACI. Eur Heart J Cardiovasc Imaging 2013; 14:611-44
- MATSUMARA Y, FUKUDA S, TRAN H. Geometry of the proximal isovelocity surface area in mitral regurgitation by 3-dimensional color Doppler echocardiography: difference between functional mitral regurgitation and prolapse regurgitation. Am Heart J 2008; 155:231-8
- PU L, VANDERVOORT PM, GRIFFIN BP, et al. Quantification of mitral regurgitation by proximal convergence method using transesophageal echocardiography. Clinical validation of a geometric correction for proximal flow constraint. Circulation 1995; 92:2169-77
- QUINONES MA, OTTO CM, STODDARD M, et al. Recommendations for quantification of Doppler echocardiography: A report from the Doppler Quantification Task Force of the Nomenclature and Standards Committee of the American Society of Echocardiography. J Am Soc Echocardiogr 2002; 15:167-84
- ROSSI A, DUJARDIN KS, BAILEY KR, et al. Rapid estimation of regurgitant volume by the proximal isovelocity surface area method in mitral regurgitation: Can continuous-wave Doppler echocardiography be omitted ?. J Am Soc Echocardiogr 1998; 11:138-48
- SIMPSON IA, SHIOTA T, GHARIB M, et al. Current status of flow convergence for clinical applications: Is it a leaning tower of “PISA” ? J Am Coll Cardiol 1996; 27:504-9
- TRIBOUILLOY C, SHEN WF, QUERE JP, et al. Assessment of severity of mitral regurgitation by measuring regurgitant jet width at its origin with transesophageal Doppler color flow imaging. Circulation 1992; 85:1248-53
- YOSEFY C, LEVINE RA, SOLIS J, et al. Proximal flow convergence region as assessed by real-time 3-dimensional echocardiography: challenging the hemispheric assumption. J Am Soc Echocardiogr 2007; 20:389-96
- ZOGHBI WA, ADAMS D, BONOW RO, et al. Recommendations for noninvasive evaluation of native valvular regurgitation: a report from the ASE developed in collaboration with the SCMR. J Am Soc Echocardiogr 2017; 30:303-71
25. Echocardiographie transoesophagienne 1ère partie
- 25.1 Introduction
- 25.2 Principes physiques de l'échocardiographie
- 25.3 Anatomie fonctionnelle
- 25.3.1 Technique et risques de l'ETO
- 25.3.2 Examen standard 2D
- 25.3.3 Examen des valves
- 25.3.4 Examen bidimensionnel des ventricules
- 25.3.5 Examen des oreillettes
- 25.3.6 Mode TM
- 25.3.7 Examen Doppler
- 25.3.8 Examen tridimensionnel (3D)
- 25.3.9 Mesures quantitatives
- 25.3.10 Examen rapide
- 25.3.11 Images artéfactuelles
- 25.3.12 Rapport d'examen
- 25.4 Mesures hémodynamiques
- 25.5 Fonction systolique du VG
- 25.6 Fonction diastolique du VG
- 25.7 Fonction ventriculaire droite
- 25.8 Fonction ventriculaire segmentaire
- 25.9 Insuffisance cardiaque
- 25.10 Place de l'ETO en clinique
- 25.11 ETO en chirurgie cardiaque
- 25.12 ETO en chirurgie non-cardiaque
- 25.13 Echocardiographie en soins intensifs
- 25.14 Echocardiographie au déchocage
- 25.15 Echocardiographie transthoracique
- 25.16 Conclusions





























